The pH scale - Strong acids and Weak acids
By: HWC
Date Uploaded: 10/18/2019
Tags: The pH scale • Expresses concentration of H+. • range: 0-14. • 7 is neutral. • Less 7 is acid. • greater 7 is basic (alkaline). Strong acids - role in the body ■ In strong acids all molecules dissociate. ■ HC1 is highly acidic and found only in the stomach. • HC1 in gastric juice is important for the digestion of proteins. • HCl kills bacteria in food by destroying their proteins. Weak acids - role in the body ■ Carbonic acid is produced from CO2 and H2O. ■ H2CO3 which helps regulate blood pH is a weak acid. • Few molecules dissociate because a strong attraction exists between H+ and HCO5. درجة الحموضة: ھو مقیاس لتحدید تركیز أیونات الھیدروجین +H في المحلول یُرمز لدرجة الحموضة بالرمز (pH) وتُعرف أیضاً بالرقم الھیدروجیني أو الأس الهيدروجيني . درجة الحموضة مقیاس مدّرج من 0 إلى 14 ویُعبّر عن تركیز أیونات +H وأیونات -OH في المحلول. فالمحالیل الحمضیة تمتلك قیمة pH أقل من (7)، وكلما قلت قیمة pH للحمض زادت قوتھ. والمحالیل القاعدیة تمتلك قیمة pH أكبر من (7)، وكلما زادت قیمة pH للقاعدة زادت قوتھا. أما الماء المقطر فتبلغ قیمة pH لھ (7)، أي أنھ یُعتبر متعادلاً وفق ھذا المقیاس لأن تركیز أیونات-OH مساٍو لتركیز أیونات +H تعتمد قيمة PH للمحلول على تركيز كل من أيون الهيدروجين الموجب H+ وأيون الهيدروكسيد السالب OH-
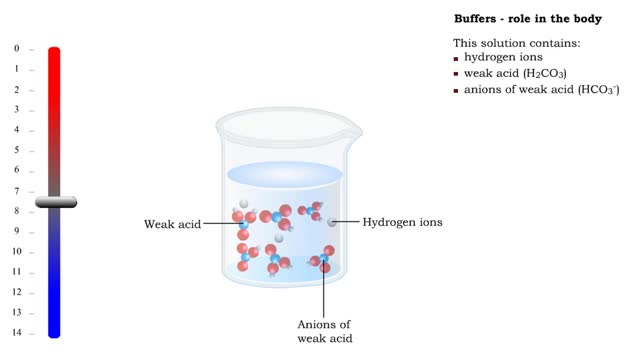
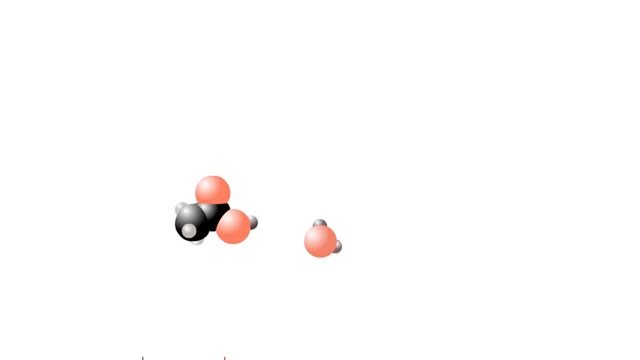
The pH scale • Expresses concentration of H+. • range: 0-14. • 7 is neutral. • Less 7 is acid. • greater 7 is basic (alkaline). Strong acids - role in the body ■ In strong acids all molecules dissociate. ■ HC1 is highly acidic and found only in the stomach. • HC1 in gastric juice is important for the digestion of proteins. • HCl kills bacteria in food by destroying their proteins. Weak acids - role in the body ■ Carbonic acid is produced from CO2 and H2O. ■ H2CO3, which helps regulate blood pH, is a weak acid. • Few molecules dissociate because a strong attraction exists between H+ and HCO5. درجة الحموضة: ھو مقیاس لتحدید تركیز أیونات الھیدروجین +H في المحلول یُرمز لدرجة الحموضة بالرمز (pH) وتُعرف أیضاً بالرقم الھیدروجیني أو الأس الهيدروجيني . درجة الحموضة مقیاس مدّرج من 0 إلى 14 ویُعبّر عن تركیز أیونات +H وأیونات -OH في المحلول. فالمحالیل الحمضیة تمتلك قیمة pH أقل من (7)، وكلما قلت قیمة pH للحمض زادت قوتھ. والمحالیل القاعدیة تمتلك قیمة pH أكبر من (7)، وكلما زادت قیمة pH للقاعدة زادت قوتھا. أما الماء المقطر فتبلغ قیمة pH لھ (7)، أي أنھ یُعتبر متعادلاً وفق ھذا المقیاس لأن تركیز أیونات-OH مساٍو لتركیز أیونات +H تعتمد قيمة PH للمحلول على تركيز كل من أيون الهيدروجين الموجب H+ وأيون الهيدروكسيد السالب OH-
Add To
You must login to add videos to your playlists.
Advertisement





Comments
0 Comments total
Sign In to post comments.
No comments have been posted for this video yet.