Enzyme structure - Properties of enzymes
By: HWC
Date Uploaded: 10/19/2019
Tags: homeworkclinic.com Homework Clinic HWC Enzyme structure catalyze reactions apoenzyme cofactor organic molecule coenzyme substrate active site Properties of enzymes reaction rate ate of synthesis of enzymes inactive enzymes الإنزيمات
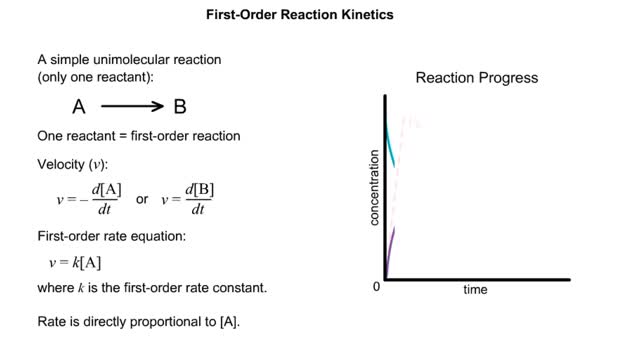
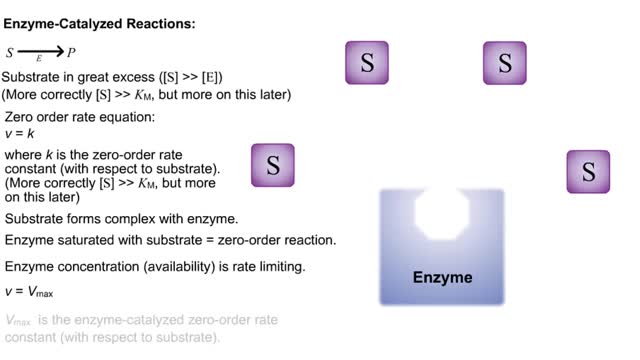
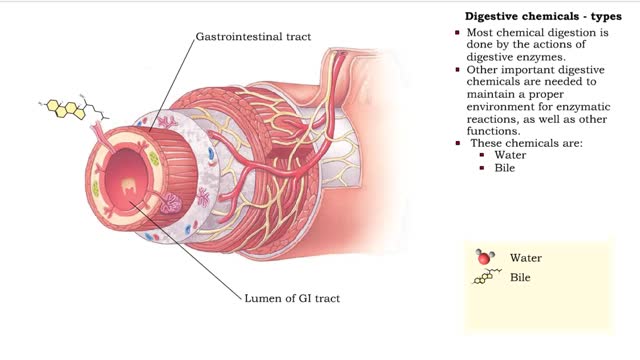
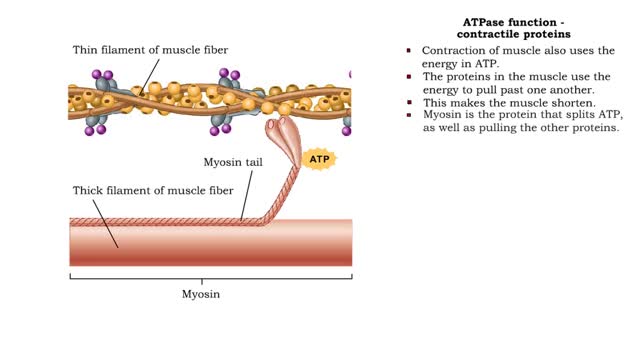
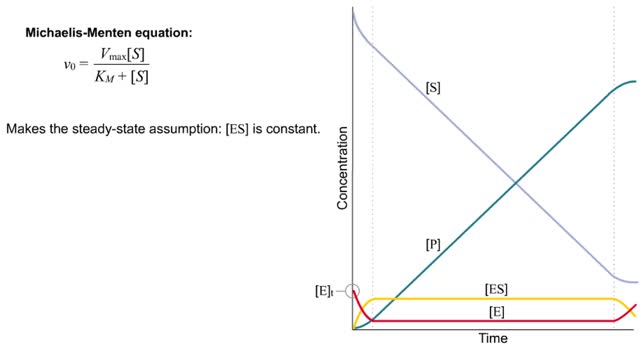
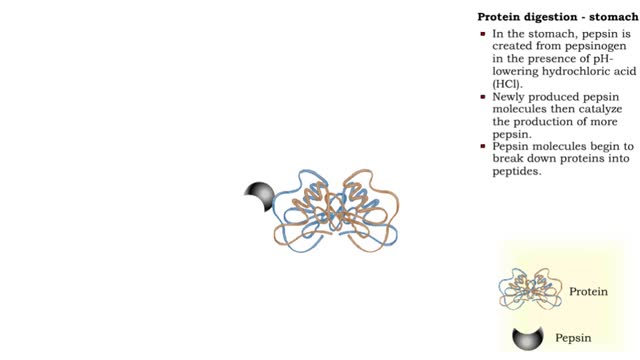
■ Enzymes are proteins that catalyze reactions. ■ Some enzymes have two parts: a protein or apoenzyme and a non-protein or cofactor. ■ Cofactor can be a metal ion or another organic molecule called a coenzyme. ■ Coenzymes often come from vitamins. ■ Cofactors affect the shape of an enzyme. ■ Cofactors allow an enzyme to carry out the reaction it catalyzes. ■ A substrate is the molecule that is acted upon by the enzyme. ■ The active site is the region of the enzyme that acts on the substrate. Enzymes have three important properties. • Enzymes are highly specific because of the close fit between the substrate and the active site. • Enzymes can increase the reaction rate more than 10 million times faster than it would occur without enzymes. Most enzymes can process more than 10,000 substrate molecules in one second. • Genes control the concentration and rate of synthesis of enzymes. • Enzyme activity can be inhibited or enhanced by substances within the cell, changing the active site or making it inaccessible. • Active or inactive enzymes are turned on or off by their chemical surroundings. • Inactive digestive enzymes in the stomach are activated when hydrogen ions break bonds in the enzyme and part of the molecule falls off, exposing the active site. الإنزيمات تُعرّف الإنزيمات بأنّها بروتينات تعمل كمحفزٍ داخل الخلايا الحية، حيث تؤدي هذه المحفزات إلى زيادة معدل حدوث التفاعلات الكيميائية، دون الاستهلاك أو التغير من شكلها، حيث إنّ التفاعل الكيميائي هو عبارة عن عملية اتحاد مادةٍ أو أكثر من المواد الكيميائية، مثل الكواشف، مع مادة من نوع آخر المنتج، حيث يعمل الإنزيم على تسهيل التفاعل الكيميائي كمحفزٍ له. تركيبة الإنزيم يتكون الإنزيم من واحدةٍ أو أكثر من سلاسل الأحماض الأمينية المترابطة الطويلة، ويمتلك كلّ إنزيمٍ تسلسلاً فريداً من الأحماض الأمينية، التي تجعل منه شكلاً مميزاً، ويتمّ تحديد تسلسل إنزيم الحمض الأميني من جينٍ معينٍ في نواة الخلية، حيث يحتوي كلّ جين من النوع نفسه على نفس النسخة من الإنزيم، كما يوجد على سطح كلّ إنزيم شق يسمى الموقع النشط، ويُمكن للمواد الكيميائية فيه، مثل الكواشف أن تتفاعل، فالإنزيم يستوعب نوعاً معيناً من الكواشف، ونوعاً معيناً من التفاعلات، إذ أنّ كلّ إنزيم مسؤول عن نوعٍ واحدٍ فقط من التفاعل الكيميائي الذي يُمكن تحفيزه. عمل الإنزيم تُقاس كفاءة نشاط الإنزيم بمعدل الدوران 106، حيث يقيس معدل الدوران عدد الجزيئات من المركب الذي يعمل فيه الإنزيم لكلّ جزيءٍ في الثانية، مثل: إنزيم الكربونيك أنهيدراز، الذي يزيل ثاني أكسيد الكربون من الدم، عن طريق ربطه بالماء، كما أنّ جزيء واحد من الإنزيم يمكن أن ينتج مليون جزيء من ثاني أكسيد الكربون في الثانية الواحدة، وتحدث معظم التفاعلات الإنزيمية تحت درجة حرارةٍ معينة تتراوح بين 30-40 درجة مئوية، وهي ميزة تعكس مدى تعقيدها كجزيئاتٍ بيولوجية.
Add To
You must login to add videos to your playlists.
Advertisement





Comments
0 Comments total
Sign In to post comments.
No comments have been posted for this video yet.